Comprendre l’impact de la mutation C9orf72 pour trouver une nouvelle approche thérapeutique
Les résultats du projet d’une durée de deux ans sélectionné en 2013 d’Adrian Isaacs.
Le Professeur Adrian Isaacs dirige un laboratoire de recherche dans le département des maladies neurodégénératives au sein de l’University College of London (UCL). UCL regroupe plusieurs équipes de pointes travaillant spécifiquement et en étroite collaboration sur la SLA.
Importance de la mutation C9orf72
Depuis la découverte de la première mutation liée à la SLA (mutation SOD1 – superoxyde dismutase de type 1) en 1993, 20 autres mutations ont été identifiées dont une mutation particulièrement intéressante sur le gène C9orf72 (portée par le chromosome 9 dans une région qui régule l’expression de ce gène appelée open reading frame 72) en 2011. Si cette mutation est la plus fréquente (environ 45%) des formes familiales, elle est aussi retrouvée dans presque 10% des formes sporadiques, ce qui en fait également la plus fréquente des causes sporadiques. L’anomalie consiste en une expansion d’une séquence de 6 bases d’ADN (GGGGCC) très inhabituelle passant de quelques copies (moins de 20 chez une personne saine) à plus de 1000 copies.
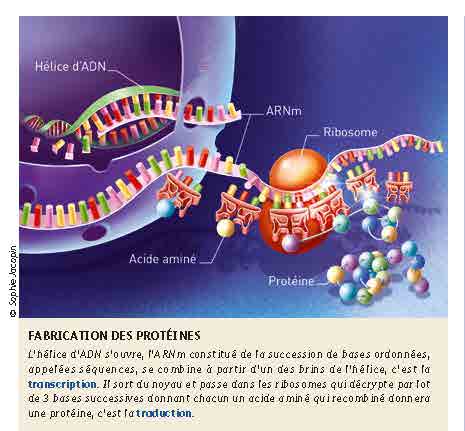
L’ADN (Acide DésoxyriboNucléique) qui se situe dans le noyau cellulaire est ensuite transcrit par des enzymes spécifiques en une molécule d’ARN (Acide RiboNucléique) spécifique qui est le messager de l’information génétique.
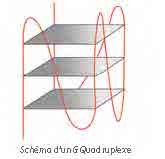
L’équipe d’Adrian Isaacs a montré que ces expansions d’ADN sont transcrites en ARN, qui copient les séquences de 6 bases formant ainsi des milliers de copies de GGGGCC. Ces expansions anormales d’ARN se plient dans une structure secondaire nommées G Quadruplexe.
Cette structure est constituée l’empilement de carrés formés par 4 molécules de G (Guanine) fixées les unes aux autres par une épine dorsale de brin d’ARN.
Ils ont ensuite démontré que ces expansions d’ARN étaient traduites en protéines répétitrices extrêmement neurotoxiques.
Le projet sélectionné en 2013 visait à rechercher comment neutraliser les structures G Quadruplexes pour diminuer la production de protéines toxiques.
Ils ont réalisé un screening de molécules pour identifier des composés ciblant spécifiquement l’ARN G-quadruplex de C9orf72 et ont identifié trois composés avec des structures chimiques semblables qui ont pu lier sélectivement cet ARN.
Ils ont ensuite testé ces molécules sur deux modèles :
Un modèle animal de mouches portant la mutation C9orf72
Des neurones dérivés des cellules souches pluripotentes crées à partir de cellules de peau de patients porteurs de la mutation C9orf72.
Dans ces deux modèles l’administration de ces molécules a permis de réduire le niveau de protéines toxiques. De plus la survie des mouches a été prolongée.
Ces résultats fournissent une preuve de principe que le ciblage de l’ARN de répétition C9orf72 GGGGCC G-quadruplex est une stratégie de traitement potentielle de la sclérose latérale amyotrophique.

Le Pr Adrian Isaacs commente ces résultats qui viennent d’être publiés :
« C’est notre travail principal issu du financement de la Fondation Thierry Latran, ces résultats sont le fruit d’un effort majeur de notre équipe en collaboration avec le département pharmaceutique d’UCL donc je suis très heureux de le voir publié dans une revue prestigieuse. »

